opredelitev periodičnega prava
 The periodični zakon je on temelj periodnega sistema elementov, kot univerzalna shema, ki organizira, razvršča in distribuira različne obstoječe kemijske elemente glede na njihove značilnosti in lastnosti.
The periodični zakon je on temelj periodnega sistema elementov, kot univerzalna shema, ki organizira, razvršča in distribuira različne obstoječe kemijske elemente glede na njihove značilnosti in lastnosti.
Osnova, na kateri sedi periodni sistem elementov
Medtem periodični zakon določa, da so fizikalne in kemijske lastnosti prej omenjenih elementov so nagnjeni k sistematičnemu ponavljanju, ko se atomsko število elementov poveča.
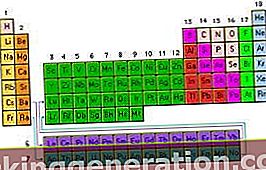
Periodična tabela: organizacija kemijskih elementov v naraščajočem zaporedju glede na število atomov, ki jih ima vsak od njih
Tako znana tabela elementov, ki jih preučujemo v šoli, pri predmetih fizike in kemije, je shema, ki se ukvarja z urejanjem kemičnih elementov glede na njihov naraščajoč vrstni red glede na število atomov.
Navpični stolpci tabele se imenujejo skupine in vsebujejo elemente z enako atomsko valenco in imajo zato podobne lastnosti, medtem ko vodoravne vrstice, imenovane pike, združujejo elemente z različnimi lastnostmi, vendar imajo podobne mase.
Kako je to znanje napredovalo: specifični in postopni dogodki
Treba je opozoriti, da so se vsi ti pojmi, ki so značilni za fiziko in kemijo, v devetnajstem stoletju razvijali postopoma in postopoma.
Povedati moramo, da so nekateri elementi, kot so srebro (Ag), zlato (Au), baker (Cu), svinec (Pb) in živo srebro (Hg), že od nekdaj imeli popolno znanje, zgodilo se je prvo znanstveno odkritje elementa v sedemnajstem stoletju, ko je alkimist Henning Brand prvič identificiral element fosfor (P).
V naslednjem stoletju, torej v 18. stoletju, so začeli poznati nove elemente, najpomembnejši pa so bili plini, zahvaljujoč razvoju pnevmatske kemije, vključno s kisikom (O), dušikom (N) in vodikom (H).
Približno v tem času je francoski kemik Antoine Lavoisier napisal seznam preprostih snovi, v katerih se je že pojavilo 33 elementov.
V začetku devetnajstega stoletja je izum električne baterije sprožil preučevanje novih kemijskih pojavov, kar je povzročilo odkritje več elementov, kot so alkalijske in zemeljskoalkalijske kovine.
Do leta 1830 je bilo identificiranih že 55 elementov.
Sredi devetnajstega stoletja so z izumom naprave, imenovane spektroskop, našli več elementov, zlasti tistih, povezanih z barvo, ki so predstavljali njihove spektralne črte, vključno s cezijem, talijem in rubidijem.
Spektroskop je instrument, ki se uporablja za opazovanje in doseganje spektra, saj je to posledica razpršitve vrste sevalnih, zvočnih ali valovnih pojavov.
Podobnost nekaterih elementov, predstavljenih v smislu kemijskih in fizikalnih lastnosti, je privedla do tega, da so se nekateri znanstveniki tistega časa odločili, da jih bodo sistematično razvrščali po določenih kriterijih.
Najbolj oddaljena predhodnica zadevnega zakona je znana Zakon o osmih, ki ga je razvil angleški kemik John Alexander Newlands, ki je predlagal prebujanje velike novosti, da se vsakih osem elementov znajdemo podobno.
To je bil prvi korak, da je oblikoval svojo periodično tabelo, ki je bila uradno objavljena leta 1863.
Kot da bi bil nekdo na post dirki, je rokavico v tem smislu prevzel drug kemik, v tem primeru Nemec Julius Lothar Meyer, ki je za izhodišče uporabil rezultate Newlandsa leta 1870, določil atomske prostornine elementov.
Ko je izračunal atomske teže in jih predstavil, je lahko svetu znanosti dokazal, da atomska teža pomeni povečanje fizikalnih lastnosti.
In skoraj sočasno z Meyerjevimi deli, Kemik, rojen v Rusiji, Dimitri Mendeleev objavlja prva periodna tabela, premagal Meyerja, ki bi to storil leto kasneje, zato je on tisti, ki je ostal zaslužen, da je njegov ustvarjalec.
Mendelejev bi elemente razvrstili v naraščajočem vrstnem redu glede na atomsko maso, ki jo predstavljajoMedtem je v isto kolumno postavil tiste, ki so delili neko značilnost.
Omeniti velja, da je bilo v tem času že znanih 63 elementov od 90 obstoječih.
Tabela je bila konec 19. stoletja dopolnjena z drugo skupino, imenovano nič, sestavljeno iz žlahtnih plinov.










